Usein kysyttyä
-
Kannabiodioli CBD:n turvallisuudesta kosmetiikkavalmisteissa on toistaiseksi saatavilla vasta vähän tietoa, ja turvallisuusarviointi on vielä kesken EU:ssa.
Alle on koottu tulkintoja, joita täydennetään, kun tieteellistä tietoa on käytettävissä enemmän.
Onko kannabidiolin (CBD) käyttö kosmetiikkavalmisteissa kielletty EU:n kosmetiikka-asetuksella?
Ei ole. Kannabidiolia (CBD) aineena ei mainita EU:n kosmetiikka-asetuksen liitteessä II, jossa on lueteltu kosmetiikkavalmisteissa kielletyt aineet.
Sen sijaan EU:n kosmetiikka-asetuksen liitteen II viitekohdassa 306 kielletään huumausaineiden, tarkemmin kaikki vuoden 1961 huumausaineyleissopimuksen taulukoissa I ja II mainittujen aineiden käyttö kosmetiikassa. Käytännössä tässä yhteydessä tällä viitataan kannabiksen, kannabishartsien sekä kannabisuutteiden ja -tinktuurojen sekä kannabiskasvin kukkivien tai hedelmiä kantavien latvojen, käyttöön kosmeettisissa valmisteissa. Nämä kasvin osat sisältävät kannabinoideja, esimerkiksi CBD:a ja tetrahydrokannabinolia (THC).
Euroopan unionin tuomioistuin (EUT) on tulkinnut sähkösavuketta koskeneessa asiassa C-663/18, että kasvista uutettu, puhdas CBD ei ole YK:n huumausaineyleissopimuksessa tarkoitettu huumausaine. Vastaavalla tavalla EU:n kosmetiikka-asetuksen liitteen II viitenumero 306 ei siten koske kosmetiikkavalmisteen ainesosana käytettävää ns. puhdasta CBD:a vaikka se olisi uutettu kannabiskasvista. Jos CBD on eristetty kasvista uutteena, se saattaa sisältää THC:tä pieninä määrinä, jääminä.
Kosmetiikka-asetuksen mukaan kiellettyjen aineiden pienten jäämien tahaton esiintyminen on sallittua, mutta tässäkin tapauksessa vastuuhenkilön on varmistuttava siitä, että valmiste on turvallinen. THC:n käyttö kosmetiikkavalmisteiden ainesosana on kielletty. THC on huumausaine ja talouden toimijan tulee noudattaa myös huumausainelainsäädäntöä.
Saako CBD:a sisältäviä kosmetiikkavalmisteita myydä Suomessa?
Saa myydä, jos kosmetiikkavalmisteet ovat EU:n kosmetiikka-asetuksen ja kansallisen kosmetiikkalain vaatimusten mukaisia.
Kosmetiikkavalmisteiden tulee täyttää kosmetiikka-asetuksen edellyttämät yleiset turvallisuutta koskevat vaatimukset (ks. EU:n kosmetiikka-asetus 3 ja 10 artiklat). Turvallisuuden osoittaminen kuuluu asetuksen 4 artiklan mukaisen EU-alueella sijaitsevan vastuuhenkilön velvollisuuksiin ennen kosmetiikkavalmisteiden markkinoille saattamista.
CBD:a sisältävien kosmetiikkavalmisteiden lääkkeellinen markkinointi
EU:n kosmetiikka-asetuksen 2.1 artiklan a)-alakohdassa olevan kosmetiikkavalmisteen määritelmän mukaan kosmetiikkavalmisteen käyttötarkoituksena on ihmiskehon ulkoisten osien puhdistaminen, tuoksun tai ulkonäön muuttaminen, suojaaminen tai pitäminen hyvässä kunnossa tai hajujen poistaminen.
Näin ollen valmiste, jota markkinoidaan sairauksien tai niiden oireiden parantamiseksi, lievittämiseksi tai ennaltaehkäisemiseksi tai joka on tarkoitettu nautittavaksi, hengitettäväksi tai injektoitavaksi ihmiskehoon ei ole kosmeettinen valmiste, vaikka se olisi merkitty kosmetiikkalainsäädännön mukaisesti tai kyseisestä valmisteesta olisi ilmoitettu asetuksen edellyttämät tiedot komissiolle CPNP-portaaliin.
Turvallisuusarvioinnin eteneminen
Euroopan komissio pyysi vuonna 2023 toimittamaan sellaisia tieteellisiä tietoja, joilla on merkitystä CBD:n turvallisuuden arvioinnissa (Call for data on ingredients used in cosmetic products - European Commission (europa.eu). Tietoja oli mahdollista toimittaa komissiolle syyskuuhun 2024 mennessä.
Toimitettujen tietojen perusteella komissio pyysi kuluttajien turvallisuutta käsittelevää tiedekomiteaa (SCCS) tekemään turvallisuudenarvioinnin CBD:n käytöstä kosmetiikkavalmisteissa Request for a scientific opinion on Cannabidiol (CBD) (CAS/EC No. 13956-29- 1/ 689-176-3) used in cosmetic products. SCCS:n lausunto on valmistunut syksyllä 2025. Lausunnossaan SCCS on arvioinut sekä CBD:n turvallisen enimmäispitoisuuden iho- ja suuhygieniavalmisteissa että suurimman turvallisen THC:n jäämäpitoisuuden näissä valmisteissa. Komissio voi ehdottaa sääntelytoimia SCCS:n lausunnon perusteella.
Ranska on lisäksi toimittanut Euroopan kemikaalivirastolle (ECHA) CBD:a koskevan CLP-asetuksen (EY) 1272/2008) mukaisen luokitusehdotuksen Repro 1B sen lisääntymiselle vaarallisista vaikutuksista. Kyseinen luokitusehdotus on ollut julkisessa kuulemisessa, ja on tällä hetkellä arvioitavana ECHAn riskinarviointikomiteassa. Arvioinnin takaraja on elokuussa 2026. Mikäli CBD:n Repro 1B-luokitus vahvistetaan, sen käyttö kosmeettisissa valmisteissa voitaisiin kieltää (kosmetiikka-asetus, artikla 15).
Päivitetty 23.3.2026 klo 12.19 -
EU:n lainsäädännössä ei ole erillistä laadullista luokitusta kosmetiikassa käytettäville raaka-aineille. Kosmetiikan raaka-aineita koskevat samat kemikaalisäädökset kuin muita kemikaaleja.
Kosmetiikan raaka-aineita koskee EU:n CLP-asetus, jonka vaatimusten mukaisesti raaka-aineet pitää luokitella, merkitä ja pakata.
Luokitusta, merkintöjä ja pakkaamista koskevaa CLP-asetusta ei sovelleta lopullisessa muodossaan loppukäyttäjille tarkoitettuihin kosmeettisiin valmisteisiin. Kosmeettisen valmisteen raaka-aineena oleva aine voi olla luokiteltu CLP-asetuksen mukaan, mutta kosmeettista valmistetta ei luokitella samalla tavalla kuin kemikaaliseokset CLP-asetuksen mukaan.
Kosmetiikan raaka-aineita koskevat myös kemikaaleja koskevat EU:n REACH-asetuksen vaatimukset, kuten vaatimus aineiden rekisteröinnistä, käyttöturvallisuustiedotteen toimittamisesta, rajoituksista ja lupamenettelystä. Kosmetiikan raaka-aineiden toimittaja on kemikaalin toimittaja, joka välittää tietoa kemikaalin ominaisuuksista ja turvallisesta käytöstä käyttöturvallisuustiedotteella asiakkailleen.
Markkinoille saatettavia kemikaaleja ei tarkasteta tai hyväksytä etukäteen. Jos kemikaalista pitää tehdä käyttöturvallisuustiedote, siitä on tehtävä myös kemikaali-ilmoitus Tukesin kemikaalituoterekisteriin, joka löytyy KemiDigi-palvelusta.
Kemikaalin toimittaja vastaa lainsäädännön vaatimusten täyttämisestä osaltaan, kuten kosmeettisen tuotteen valmistaja omalta osaltaan. Kemikaalin ostajan kannattaa ehkä määritellä toimittajalleen, minkälaista kemikaalia tarvitsee ja haluaa, ja pyytää tarvittaessa dokumentaatiota vaatimusten täyttymisestä.
Kosmetiikan raaka-aineiden osalta kannattaa olla selvillä kosmeettisten lopputuotteiden, kosmeettisten valmisteiden rajoituksista. Kun jokin aine saa CLP-asetuksen kriteerien mukaisen harmonisoidun luokituksen syöpää aiheuttavaksi, perimää vaurioittava, lisääntymiselle vaaralliseksi, eli CMR-aineeksi, aine lisätään kosmetiikka-asetuksessa kiellettyjen aineiden luetteloon kosmetiikka-asetuksen liitteeseen II, joka on luettelo kosmeettisissa valmisteissa kielletyistä aineista.
Kosmetiikka-asetus rajoittaa myös muilta osin tiettyjen aineiden käyttöä kosmeettisissa valmisteissa seuraavasti:
- liite III: luettelo aineista, joita kosmeettiset valmisteet saavat sisältää vain määrätyin rajoituksin
- liite IV: kosmeettisissa valmisteissa sallitut väriaineet
- liite V: luettelo kosmeettisissa valmisteissa sallituista säilöntäaineista
- liite VI: kosmeettisissa valmisteissa sallittujen uv-suodattimien luettelo.
Kosmeettisten valmisteiden pitää täyttää kosmetiikkalainsäädännön vaatimukset, joista voit lukea lisää kosmetiikkaa koskevalta verkkosivulta.
Kemikaalien luokituksesta CLP-asetuksen mukaisesti kerrotaan luokitusta koskevalla sivulla.
Linkki REACH-asetuksen liitteeseen XVII rajoitetuista aineista löytyy kieltoja ja rajoituksia koskevalta sivulta.
REACH-asetuksesta on mm. kaksi nimikettä, nimikkeet 46 ja 70, joissa aineiden käyttöä on rajoitettu kosmeettisissa valmisteissa aineiden aiheuttaman ympäristövaaran takia.
Lue lisää REACH-asetuksen luvanvaraisista aineista.
Lue lisää käyttöturvallisuustiedotteesta.
Lue lisää kemikaali-ilmoituksesta.
C&L-tietokannasta Euroopan kemikaaliviraston sivulla voi hakea aineita ja niiden luokituksia esimerkiksi aineen englanninkielisen kemiallisen nimen, nimen osan tai CAS-numeron avulla.
Kootusti tietoa REACH- ja CLP-asetuksien velvoitteista löydät toimijoiden REACH- ja CLP-velvoitteista kertovalta verkkosivulta.
-
EU:n kosmetiikka-asetusta sovelletaan kosmeettisiin valmisteisiin, jotka on tarkoitettu saatettavaksi markkinoille. EU:n kosmetiikka-asetuksessa ”asettamisella saataville markkinoilla” tarkoitetaan kosmeettisen valmisteen toimittamista yhteisön markkinoille liiketoiminnan yhteydessä jakelua, kulutusta tai käyttöä varten joko maksua vastaan tai maksutta. Lainsäädännön velvoitteet koskevat tältä osin yhtälailla yrityksiä kuin yksityisiä henkilöitäkin.
Kun saippuaa toimitetaan jakelua, kulutusta tai käyttöä varten joko maksua vastaan tai maksutta liiketoiminnan yhteydessä, tulee sen täyttää kosmetiikkalainsäädännön vaatimukset. Jos myyt saippuoita säännöllisesti pieninäkin määrinä, voidaan toiminnan katsoa olevan liiketoimintaa ja näin ollen lainsäädännön velvoitteet on täytettävä.
Lainsäädäntö ei ota tarkempaa kantaa siihen, mikä on tai ei ole kosmetiikkalainsäädännön tarkoittamaa liiketoimintaa, Tukesin valvontaviranomaisena tekemän tulkinnan mukaan kosmetiikkalainsäädännön piiristä rajautuvat pois ne toimijat, jotka valmistavat saippuaa omaan käyttöön tai antavat saippuoita lahjaksi ystävilleen (poislukien liikelahjat). Lisäksi omatekoisen saippuan satunnaisen myynnin yksittäisissä tapahtumissa pieninä määrinä ei katsota olevan liiketoimintaa.
Tällaisia tapahtumia, joissa omatekoisen saippuan pienimuotoista satunnaista myyntiä ei katsota liiketoiminnaksi, voivat olla esimerkiksi koululuokan tai urheiluseurojen järjestämät myyjäiset tai joulumyyjäiset, jos toiminta ei ole säännöllistä ja myytävien saippuoiden määrä on pieni.
Velvoitteiden noudattamista on arvioitava aina tapauskohtaisesti huomioiden mm. toiminnan säännöllisyys ja jaeltavien tuotteiden lukumäärä ja jakelun laajuus. Saippuoiden myynti ja markkinointi omalla toiminimellä on aina liiketoimintaa. Tähän sisältyy myös saippuoiden myynti verkkosivujen kautta tai myymälöissä.
Jos teet saippuoita harrastuksena, Tukes suosittelee, että annat saippuan mukana aina tiedot valmisteen sisältämistä ainesosista. Näin saippuan käyttäjä voi välttää niiden valmisteiden käyttöä, jotka sisältävät hänelle sopimattomia ainesosia esimerkiksi allergioiden vuoksi. Muista myös, että jos saippuan käyttäjä saa tuotteesta oireita, valmistaminen harrastustoimintana ei poista vastuuta ostajaan nähden tälle aiheutuneesta mahdollisesta haitasta tai vahingosta.
Oikeusperusta: EU:n asetus kosmeettisista valmisteista (EY) N:o 1223/2009 2 artikla g alakohta
Yhteenveto tärkeimmistä lainsäädäntöön perustuvista velvoitteista kosmetiikkaa valmistettaessa ja markkinoille saatettaessa joko Suomessa tai muualla Euroopassa:
1) turvallisuusselvityksen laatiminen EU:n ohjeistusten mukaisesti,
2) tuotteen ilmoittaminen komission sähköiseen tietokantaan (CPNP),
3) pakkausmerkintöjen laatiminen sen EU:n jäsenvaltion kansallisen lainsäädännön vaatimusten mukaisesti, jossa valmiste asetetaan loppukäyttäjien saataville (Suomessa Lain kosmeettisista valmisteista 492/2013),
4) kosmetiikka-asetuksen liitteissä II-VI esitettyjen kosmeettisen valmisteen ainesosia koskevien vaatimusten ja rajoitusten noudattaminen,
5) tuotteen valmistamisen hyvää valmistustapaa noudattaen, esimerkiksi tätä koskevan ISO 22716:2007 standardin mukaisesti. GMP-standardi on saatavana myös suomeksi SFS Suomen Standardit ry:stä. (www.sfs.fi) Kts. tarkemmin kohta 3. Mitä kosmetiikkalainsäädäntö edellyttää.
-
Yksittäisten yrittäjien, työväenopistojen tai niiden kaltaisten toimijoiden järjestämät kosmetiikan valmistuksen kurssit ovat kuluttajille tarjottavia palveluja, ja kurssille osallistuvien kuluttajien turvallisuudesta vastaa palveluntarjoaja. Palveluntarjoajan tulee mm. varmistaa palvelun turvallisuus sekä se, että tarjottavasta palvelusta ei aiheudu vaaraa kenenkään terveydelle.
Lue lisää: Tukesin verkkosivut vapaa-ajan palvelujen turvallisuudesta ja laki kulutuspalvelujen turvallisuudesta (185/2025)
Anna osallistujalle tarvittavat turvallisuustiedot
Kuluttajalle pitää antaa kaikki palvelun turvallisuuden kannalta olennaiset tiedot, jotta hän voi arvioida mahdollisuutensa osallistua palveluun. Käytännössä tämä tarkoittaa, että palveluntarjoaja kartoittaa palvelun sopivuuden kuluttajalle ja käy läpi tarvittavat turvallisuusasiat. Esimerkiksi seuraavilla kysymyksillä pääsee alkuun kosmetiikkakurssin turvallisuuden suunnittelussa:
- Onko jokin asiakasryhmä, jolle kurssi ei sovi?
- Millaisia tietoja käsiteltävistä aineista on tarpeen antaa ennakkoon, esim. allergisille?
- Millaisia riskejä kurssiin liittyy ja miten näitä ennaltaehkäistään?
- Millaiset perehdytysohjeet tarvitaan? Miten perehdytys suoritetaan (suullisesti, kirjallisesti)?
- Käsitelläänkö laitteita tai aineita, joiden käyttö edellyttää ohjeistusta tai ohjeita? Huomioon on hyvä ottaa esim. kiehuva vesi, kemikaalit, sähkölaitteet ym.
- Miten asiakkaat suojautuvat? Käsineet, hengityssuojaimet, suojalasit, suojavaatteet?
Kurssinpitäjän on siis etukäteen perehdyttävä kurssilla käytettävien raaka-aineiden ominaisuuksiin sekä tunnettava niihin liittyvät mahdolliset riskit kosmetiikkakäytössä ja miten niiltä suojaudutaan. Palvelun turvallisuus tulee dokumentoida.
Mitkä vaatimukset koskevat kurssilla valmistettavaa kosmetiikkaa?
EU:n kosmetiikka-asetuksen vaatimukset eivät koske kaupallisilla tai työväenopiston kursseilla omaan käyttöön valmistettavia kosmetiikkavalmisteita. Kun osallistuja valmistaa kurssin aikana omaan käyttöön kurssilla tarjottavista erilaisista raaka-aineista kosmetiikkavalmisteita kurssilla annettavien ohjeiden mukaan, kyseessä ei ole kosmetiikka-asetuksen mukainen kosmetiikan markkinoille saattaminen.
Valmistajalla tarkoitetaan ihmistä tai yritystä, joka valmistaa, suunnitteluttaa tai valmistuttaa kosmeettista valmistetta ja markkinoi sitä omalla nimellään tai tavaramerkillä. Jos kurssilla tai työpajassa valmistetaan kosmetiikkaa myyntiä tai muuta luovutusta varten tai jos kurssin tarkoituksena on samalla myydä valmistettavat tuotteet, tulee kosmetiikkalainsäädäntö sovellettavaksi. Tällöin myös kaupallisesti toimiva palveluntarjoaja voi olla kosmetiikkavalmisteen EU:n kosmetiikka-asetuksen mukainen valmistaja ja samalla tuotteen vastuuhenkilö. Vastuuhenkilö on vastuussa siitä, että kursseilla valmistettavat valmisteet täyttävät kaikki kosmetiikkalainsäädännön vaatimukset. Kurssille osallistuneesta taas tulee valmistaja, jos hän luovuttaa omissa nimissään valmistamaansa kosmetiikkaa eteenpäin ja toiminta rinnastuu liiketoimintaan. Katso opas Harrastajan korut ja kosmetiikka.
Kurssille/työpajaan osallistuvalle tulisi kertoa etukäteen siitä, että kursseilla valmistettava kosmetiikka on tarkoitettu vain omaan käyttöön ja ottaa esille, jos se ei sellaisenaan ole EU:n kosmetiikka-asetuksen vaatimusten mukaista, eikä sitä voi kaupallistaa tai muutoin jaella ilman tarkempaa turvallisuusarviointia. Kurssin pitäjä voi vapaaehtoisesti teettää kurssilla valmistettavaksi suunnitelluille valmisteille EU:n kosmetiikkalainsäädännön mukaisen turvallisuusarvioinnin asiantuntijalla. Sitä voi samalla käyttää kuluttajaturvallisuuslain edellyttämän palveluntarjoajan huolellisuusvaatimuksen täyttämiseksi.
Jos kursseilla käytetään valmista kosmetiikkaa tai muita tuotteita tai osallistujille lahjoitetaan tuotteita/kosmetiikkaa, tulee niiden olla sovellettavan tuotelainsäädännön mukaisia.
EU:n kosmetiikka-asetus (EY) N:o 1223/2009
Valmistajan määritelmä: EU:n kosmetiikka-asetuksen 2 artiklan 1 kohdan alakohta d)
-
Kosmetiikkatuotteessa pitää olla seuraavat pakkausmerkinnät:
- käyttötarkoitus, ellei se käy ilmi pakkauksesta tai tuotteen nimestä
- EU-alueella toimivan vastuuhenkilön tiedot
- sisällön määrä
- ainesosaluettelo
- tuotteen säilyvyys
- mahdolliset varoitukset tai muut turvallista käyttöä koskevat ohjeet, mikäli tuotteen turvallinen käyttö sitä edellyttää
- eränumero tai muu tunniste
- alkuperämaa, jos tuote on tuotu EU:n ulkopuolelta
-
Jos tuotteessa on hajusteita, ne on merkitty ainesosaluetteloon termillä parfum tai aroma. Mikäli valmiste sisältää herkistäväksi tunnistettuja hajusteraaka-aineita, ne merkitään termin parfum tai aroma lisäksi omilla INCI-nimillään. Niin sanotut INCI-nimet ovat yhteinen kosmeettisten ainesosien nimistö, joka on käytössä EU-alueella.
-

Symboli tarkoittaa, että tuotteeseen kiinnitetystä tai sen mukana tulevasta liitteestä löytyy lisätietoa.
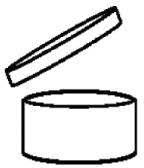
Symboli kertoo tuotteen säilyvyyden avaamisen jälkeen. Kuvan sisällä oleva luku kertoo, montako kuukautta tuote säilyy avattuna. Esimerkiksi 12M viittaa 12 kuukauteen.

Symboli kertoo tuotteen vähimmäissäilyvyysajasta, eli mihin asti valmiste on käyttökelpoinen. Ajankohta ilmoitetaan muodossa kk/vvvv tai pv/kk/vvvv.
-

Symboli on hiusväreissä käytettävä varoitusmerkki.
Symboleiden lisäksi tuotteet voivat sisältää sanallisia varoituksia, joita ei ole erikseen korostettu varoitusmerkillä.
-
Mikäli tuote aiheuttaa vakavan ei-toivotun vaikutuksen, voit tehdä ilmoituksen tuotteen ostopaikkaan. Jakelijoilla ja vastuuhenkilöillä on lakisääteinen velvollisuus ilmoittaa heidän tietoonsa tulleet kosmetiikan aiheuttamat vakavat ei-toivotut vaikutukset valvontaviranomaiselle. Vakavia vaikutuksia ovat väliaikainen tai pysyvä toimintahäiriö, vammautuminen, joutuminen sairaalahoitoon, synnynnäinen kehityshäiriö, välitön hengenvaara tai kuolema.